Wat zijn de beperkingen van iontoforese?
Bij iontoforese worden geneesmiddelen door de huid gedrukt door een elektrische stroom, maar er zijn ook beperkingen. Veel bewijs voor de werkzaamheid is er eigenlijk nog niet. En duur is het zeker. Het blijkt dat lokale pijnstillende crèmes vermoedelijk beter zijn.

Iontoforese is niet nieuw. Als je de geschiedenis van de iontoforese bekijkt, kom je de volgende auteurs tegen:
Benjamin Ward Richardson (1828-1896), Hermann Munk (1839-1912), William James Morton (1846-1920), Stéphane Leduc (1853-1939) en Fritz Frankenhäuser (1868). De geschiedenis is mooi beschreven, maar nu de inhoud.
Wat is iontoforese?
Onder de kathode (negatieve pool) worden negatief geladen ionen van een geneesmiddel of pijnstillend middel als het ware door de huid gedreven.
In de wetenschap wordt iontoforese gewichtig omschreven als “het ondersteunen van de verplaatsing van ionen door een membraan heen, met behulp van een extern aangebracht potentiaalverschil”.
Geneesmiddelen toedienen via de huid?
Het gaat om een techniek van toediening van een geneesmiddel of een pijnstiller, waarbij de stof door de huid getransporteerd wordt (transdermaal) met behulp van een lichte, duidelijk voelbare stroom.
Het gevoel heeft wat weg van prikkeldraad, het pestspelletje van vroeger, waarbij je de huid in een tegengestelde richting op de arm draaide. De Iontoforese techniek wordt gebruikt voor stoffen die normaal niet door de huid kunnen komen, maar als ion een extra drijfkracht hebben: dat noemen we de elektrische potentiaal.
Door de hoeveelheid stroom optimaal te kiezen, kan de toegediende dosis ook worden aangepast, variërend van patiënt tot patiënt. Zo is dit een vorm van ‘geïndividualiseerde therapie’.
Iontoforese pleisters werken op een batterij, het principe lijkt een beetje op een TENS.
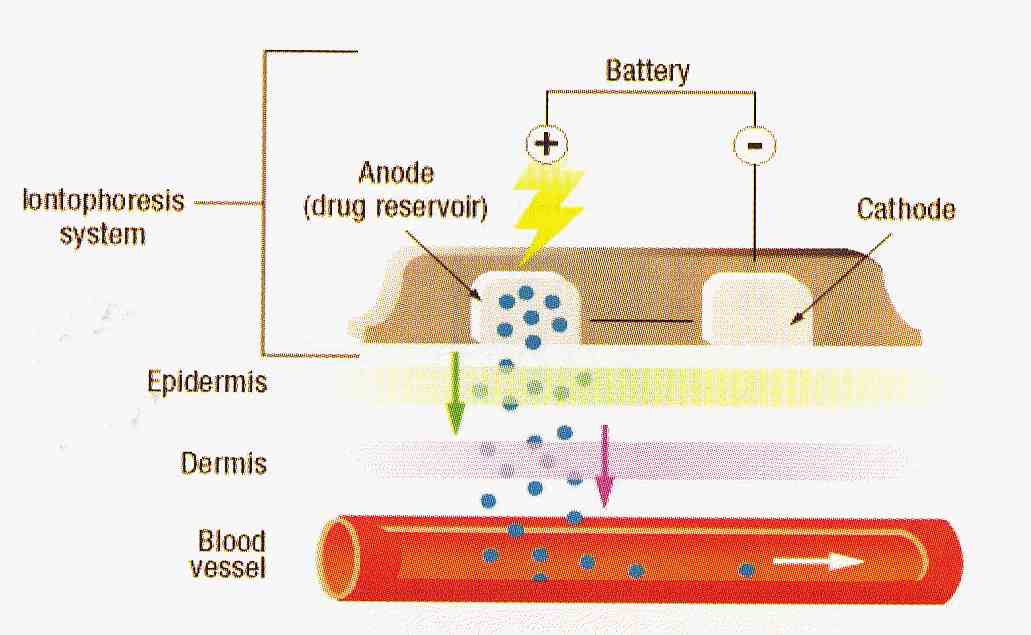
Theorie iontoforese
De theorie achter de iontoforese-pleisters is vrij simpel. Als bij de positieve pool het medicijn zich in ion-vorm bevindt dat eveneens een positieve lading bevat, zal bij het aanzetten van de stroom die stof via de huid zich naar de negatieve pool bewegen.
Na transport door de huid heen stoot het molecuul op een bloed- of lymfevat. En zal zo dus afgevoerd worden en in het hele lichaam zich verdelen in een hele lage dosering. Ook lokaal op de huid heeft de stof als het een pijnstillende stof is meteen invloed op de zenuwuiteinden.
In een vergelijkende studie bleek iontoforese met een pijnstiller tenminste beter te zijn dan TENS alleen.[1] En het is met een sterke pijnstiller even effectief als een morfine pomp.[2][3]
Ondanks dat het heel voor de hand liggend is dat men gelijkstroom dient in te zetten, zijn er ook meldingen dat wisselstroom zinvol is.[4]
De meeste studies zijn gedaan met Fentanyl. Omdat er ook al een fentanyl-pleister op de markt is, is de innovatiegraad daarvan niet zo hoog. Opvallend is dat er vrij weinig studies gedaan zijn met meer gedurfde stoffen, zoals Ketamine of Clonidine. Daarom is er nog veel te onderzoeken op dit gebied.
Enkele issues bij Iontoforese
De Indiase groep bestaande uit Swati Rawat, Sudha Vengurlekar, B Rakesh, S Jain, G Srikarti, vatten enkele beperkingen van iontoforese goed samen:
- Many factors have been shown to affect the results of iontophoresis. These include the physicochemical properties of the compound (molecular size, charge, concentration), drug formulation (types of vehicle, buffer, pH, viscosity, presence of other ions), equipment used (available current range, constant vs . pulsed current, type of electrode), biological variations (skin site, regional blood flow, age, seks), skin temperature and duration of iontophoresis.
Enkele details:
1. pH
De pH is belangrijk voor een effectieve iontoforese van medicatie. De optimale situatie van iontoforese is wanneer het medicijn hoofdzakelijk in geïoniseerde vorm aanwezig is. Hoe lager de pH, hoe hoger de concentratie van de waterstofionen (H+). Waardoor er vaatverwijding optreedt door het activeren van de C-zenuwvezels.
De optimale pH ligt rond 5,5. Wanneer vaatverwijdende medicijnen worden toegediend, kan de pH zelfs lager zijn. Het enige risico is alleen dat het vaatverwijdend effect dan vooral ligt aan de waterstofionen in plaats van aan het vaatverwijdend medicijn zelf. Omdat waterstofionen kleiner zijn dan de medicijnmoleculen. De geioniseerde staat van een medicijn ligt aan de pH en is voor ieder medicijn verschillend.
Het pH-optimum ligt dus aan het medicijn dat toegediend wordt. Er moet dus een balans gevonden worden tussen het pH-optimum van het medicijn en de aanvaardbare en veilige grens van de pH voor de patient.
2. Stroom
Er bestaat een lineaire relatie tussen de stroomsterkte en de penetratie van het medicijn per cm2. De stroomsterkte is echter beperkt tot 1 milliampère (mA), om het voor de patiënt nog comfortabel te houden. Het toedienen van de stroom zou niet langer moeten duren dan 3 minuten. Dit vanwege niet specifieke reacties als lokale huidirritatie, blaren en brandwonden. Hoe hoger de stroomsterkte des te groter de kans op vaatverwijding.
Bij een stroomsterkte van 0.4-0.5 mA/cm2, ontstaat er al een vaatverwijding na een paar seconden wanneer kraanwater of gedeioniseerd water wordt gebruikt voor iontoforese. Dit effect is waarschijnlijk het gevolg van de stroomdichtheid. Deze is groot genoeg om de uiteinden van de gevoelszenuwen te stimuleren, en zo substantie P vrij te laten maken uit de uiteinden van de C-zenuwvezels. Dit heeft vaatverwijding tot gevolg.
3. Huidpolarisatie
Het continu aanbieden van gelijkstroom gedurende een lange tijd kan de effectiviteit van de iontoforese beïnvloeden. Hoe langer er een continue gelijkstroom wordt aangeboden, des te groter de kans is dat er een grotere polarisatie van de huid ontstaat. Dit is een duidelijke beperking, want hierdoor wordt het effect van de iontoforese verminderd.
Deze polarisatie kan voorkomen worden door een gepulseerde gelijkstroom aan te bieden, dus gelijkstroom aanbieden afgewisseld met rustperioden. Zo kan in de rustfase de huid zich depolariseren. Uit onderzoek is gebleken dat bij eiwitmoleculen (peptiden en proteinen) gepulseerde iontoforese effectiever is dan continue iontoforese.
De meeste moleculen voor iontoforese die gebruikt worden voor diagnostische doeleinden, zijn klein. Hierdoor kunnen ze eenvoudiger penetreren door de huid. Het effect wordt dan vrij snel bereikt, tussen 5 en 20 seconden. Iontoforese als therapie duurt langer, 20 tot 40 minuten.
Er zijn zeker beperkingen bij iontoforese. En nog veel factoren meer. Een en ander maakt duidelijk dat je niet zo maar wat kunt doen. Goede adviezen van gespecialiseerde apothekers zijn nodig bij het verder ontwikkelen van iontoforese-systemen met verschillende pijnstillende stoffen.
4. Lokale pijnstillende crèmes als alternatief
In ons instituut hebben we een hele serie speciale pijnstillende crèmes ontwikkeld om ernstige pijn te behandelen via de huid. Dit doen wij op basis van o.a. Ketamine crème, Baclofen crème, en Gabapentine crème.
Iedere arts kan bij ons een aanvraagformulier opvragen, zodat onze apotheker voor u de crème kan afleveren. De crèmes kunnen worden vergoed door uw zorgverzekeraar.
Deze crèmes verminderen de pijn vermoedelijk beter dan via de iontoforese methodiek.
De naam van je Fibromyalgie
Fibromyalgie behandelen met Amitriptyline crème
Lidocaine pleister geregistreerd in Europa
